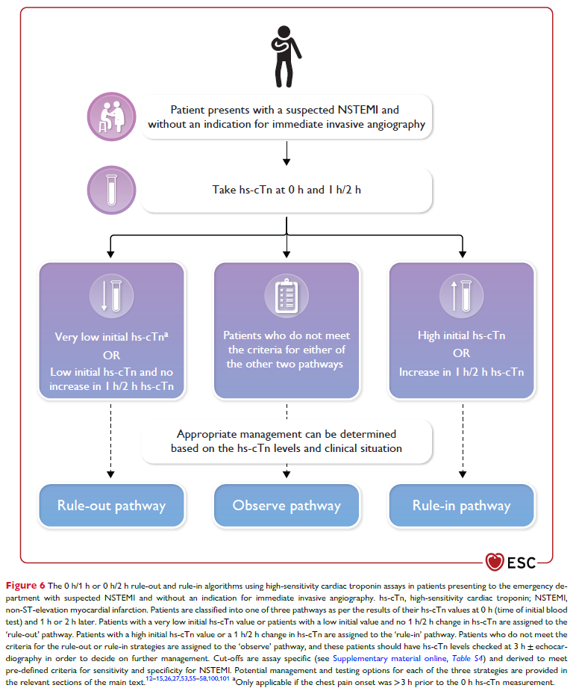
Cut-off 0 h/1 h und 0 h/2 h Algorithmus
| Aus: Byrne RA et al. 2023 ESC Guidelines for the management of acute coronary syndromes. Supplemenatry data. Developed by the task force on the management of acute coronary syndromes of the European Society of Cardiology (ESC). Eur Heart J 2023, https://doi.org/10.1093/eurheartj/ehad191 |
| In der Zentralen Einrichtung Klinische Chemie, Universitätsklinikum Ulm, wird der Assay hs-cTn T (Elecsys; Roche) verwendet. Siehe hierzu auch das Leistungsverzeichnis. |
letzte Änderung 03.01.2024
Haftungsausschluss
Jegliche Informationen wurden und werden vor ihrer Veröffentlichung mit äußerster Sorgfalt überprüft. Es wird jedoch keinerlei Gewähr für die Aktualität, Korrektheit, sachliche Richtigkeit, Vollständigkeit oder Qualität der bereitgestellten Informationen übernommen. Haftungsansprüche welche sich auf Schäden materieller oder ideeller Art beziehen, die durch die Nutzung oder Nichtnutzung der dargebotenen Informationen bzw. durch die Nutzung fehlerhafter und unvollständiger Informationen verursacht wurden, sind grundsätzlich ausgeschlossen, sofern nachweislich kein vorsätzliches oder grob fahrlässiges Verschulden vorliegt. Die Verwendung und Nutzung der Zusammenstellungen liegt daher alleine im Verantwortungsbereich des Nutzers/der Nutzerin, welche/r das Universitätsklinikum Ulm AöR gegenüber Ansprüchen Dritter schad- und klaglos halten wird (Haftungsfreistellung). Alle Veröffentlichungen sind freibleibend und unverbindlich. Es wird ausdrücklich vorbehalten, Teile der Veröffentlichung oder die gesamte Veröffentlichung ohne gesonderte Ankündigung zu verändern, zu ergänzen, zu löschen oder die Veröffentlichung zeitweise oder endgültig einzustellen.